ALK篇概要 克唑替尼(一代) 1. PROFILE 1007研究:二线,克唑替尼 vs 化疗,PFS为7.7 vs 3.0个月,ORR为65% vs 20% 2. PROFILE 1014研究:一线,克唑替尼 vs 化疗,ORR为74% vs 45%,校正OS为59.8 vs 19.2个月 3. PROFILE 1029研究(中国人群):一线,研究设计、研究结果与PROFILE 1014相似 阿来替尼(二代) 4. ALEX研究:一线,阿来替尼 vs 克唑替尼,PFS为25.7(研究者评估34.8个月) vs 10.4个月,颅内ORR为81% vs 50% 5. ALTA-3研究:克唑替尼耐药,布格替尼 vs 阿来替尼,疗效类似,布格替尼不良反应更明显;疗效对比金标准,头对头临床试验,警惕“史上最佳们”宣传 布格替尼(二代) 6. ALTA-1L研究:一线,布格替尼 vs 克唑替尼,PFS分别为24.0 vs.11.0个月,颅内ORR为78% vs26% 赛瑞替尼(二代) 7. ASCEND-3研究:二线,合并脑转移组、无脑转移组ORR为57.1% vs 74.7%,OS为36.2 vs 55.3个月 8. ASCEND-4研究:一线,赛瑞替尼 vs 化疗,PFS分别为16.6 vs 8.1个月,颅内ORR为72.7% vs 27.3% 9. ASCEND-8研究:一线,减量(450mg随餐)不减效[ASCEND-4研究(750mg)副作用明显],3年OS率高达93.1% 恩莎替尼(国产)(二代) 10. 一项II研究:二线,ORR为52%,PFS为9.6个月,颅内ORR为70% 11. eXalt 3 研究:一线,恩莎替尼 vs 克唑替尼,PFS为25.8 vs. 12.7个月,颅内ORR为54% vs 19% 劳拉替尼(三代) 12. CROWN研究:一线,劳拉替尼“碾压”克唑替尼 NVL-655(四代) 13. ALKOVE-1研究:可解决劳拉替尼耐药,希望之星 TPX-0131(四代,临床试验已终止) 耐药机制 14. 第二代能克服克唑替尼的大多数耐药突变,第三代对G1202R较为敏感,复合耐药突变几乎对所有耐药 15. 详见正文 非EML4-ALK个案报道ALK TKI疗效与EML4-ALK相近或更好,也有少部分报道与原发耐药有关。EML4-ALK占90%-95%,亚型包括:E4; A20(2.34%),E12; A20(1.56%),E13; A20(V1)(40.63%),E6; A20(V3)(36.75%),E20; A20(V2)(7.81%),E14; A20(V7)(0.78%),E18; A20(V5′)(1.56%),E15; A20(0.78%),E2; A20(V5)(0.78%),E5; A20(0.78%),E17; A20(1.56%),E3; A20(0.78%),E21; A20(2.34%),少见非A20有:E18;A17,E6; A17,E6; A18,E6; A19;E13; A19等。日本的一项回顾性研究发现35例接受克唑替尼治疗的ALK阳性肺癌患者中,EML4-ALK变体1(V1)占54%(19例),EML4-ALK 变体3a/b(V3a/b)占11 %(4例),EML4-ALK变体2(V2)占14%(5例),其它ALK变体7例。ALK 变体1组中基线脑转移比例为53%,非ALK 变体1组中为58%,二组患者的药物不良反应没有显著性差异。ALK变体1融合亚型与非变体1型相比显示更好的疗效,ORR(74% vs 63%)(P=0.7160,无显著性差异),DCR(CI:95% vs 63%)(P<0.05,有显著性差异),PFS1(1月 vs 4.2月)(P<0.05,有显著性差异)。非A20的EML4-ALK,个案报道与原发耐药耐药有关。 肺癌中非EML4-ALK类型(至少113种)占ALK融合的5%-10%:KIF5B-ALK,KLC1-ALK,HIP1-ALK,SOCS5-ALK,DCTN1-ALK,SQSTM1-ALK,SQSTM2-ALK,SQSTM3-ALK,SQSTM4-ALK,ZNF2-ALK,EXOC6B-ALK,BIRC6-ALK,CEBPZ-ALK,PICALM-ALK,TPR-ALK,CRIM1-ALK,STRN-ALK,PTPN3-ALK,CLTC-ALK,ZC3H8-ALK,ALK-LOC102723854,ALK-DTNB-ASXL2,GCC2-ALK,DYSF-ALK,LOC1720-ALK,PRKAR1A-ALK,MTA3-ALK,CLIP4-ALK,MPRIP-ALK,ITGAV-ALK,VIT-ALK,KCNQ-ALK,PPM1B-ALK,TFG-ALK,PLEKHA7-ALK,CMTR1-ALK,PHACTR1-ALK,LMO7-ALK,PICALM-ALK,BCL11A-ALK,EIF2AK3-ALK,PPM1B-ALK,DTNB-ALK,NR_110271-ALK,ZC3H8-ALK,STED2-ALK,FMNL2-ALK,CEP68-ALK,CUX1-ALK,FAM179A-ALK,SATB2-ALK,VPS54-ALK,ANKRD30BL-ALK,KIF13A-ALK,NCK2-ALK,SLC8A1-ALK,THADA-ALK,TLN2-ALK,WDFY2-ALK,ALK-LRPPRC,SRBD1-ALK,NCOA1-ALK,MEMO1-ALK,FBXO36-ALK,TPR-ALK,VKORC1L1-ALK,CAMKMT-ALK,MYT1L-ALK,GPD2-ALK,GPD2-ALK,LOC101929378-ALK,MTA3-ALK,MYT1L-ALK,TRIM66-ALK,SWAP70-ALK,WNK3-ALK,ERC1-ALK,FBN1-ALK,NYAP2-ALK, RIC8B-ALK,MIR4431-ALK,LOC102800447-ALK,ALK-CENPO,SRD5A2-ALK,LRP1B-ALK,ALK-ALMS1-IT1,ALK-GALNT14,ALK-LINC00907,ALK-PAX4,ALK-LOC101929723,ALK-BCL11A,LOC388942-ALK,LRPPRC-ALK,ALK-HTR4,ALK-FAM84A,ALK-KCNK3,ALK-NBEAL1,ALK-KCNG3,ALK-LOC90784,LCA5-ALK,LOC101927577-ALK,ADAM28-ALK,LINC01250-ALK,SLC8A1-AS1-ALK,XDH-ALK,LOC100288911-ALK,FTH1P3-ALK,NRXN1-ALK,PTGFRN-ALK,TPM3-ALK,PPFIBP1-ALK,FBXO11-ALK,ALK-KLHL29。基本情况
临床病理特点
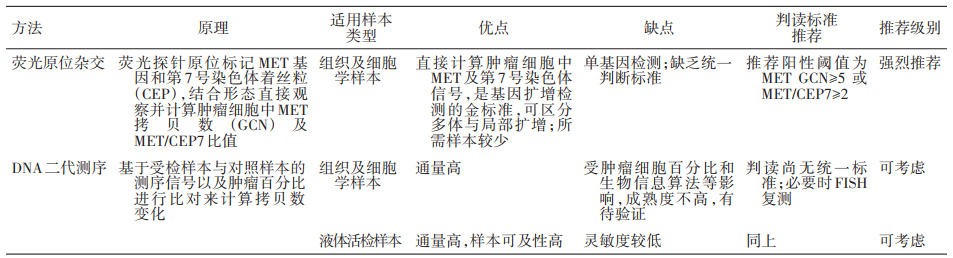
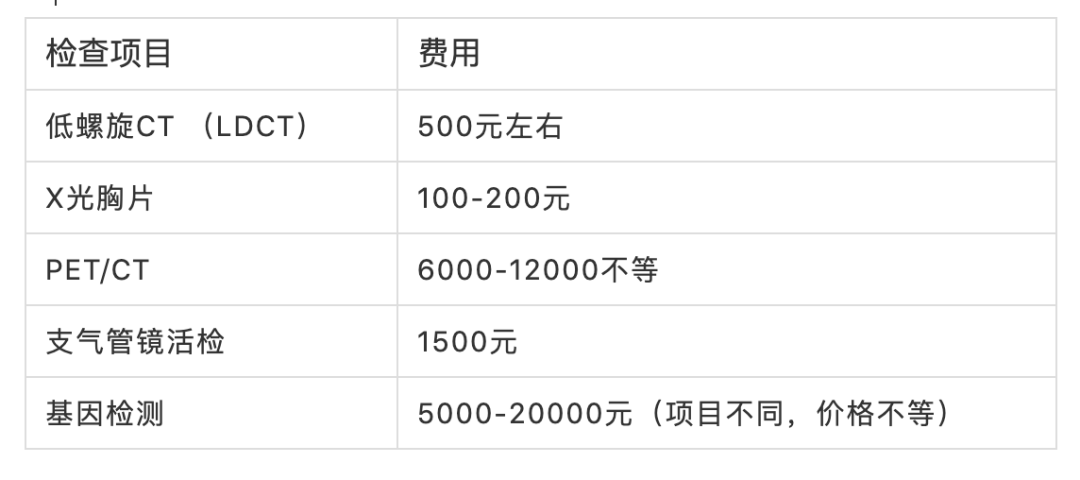
检测方法
亚型分析-了解

第一代ALK-TKIs
克唑替尼(Cizotinib)





研究结果:克唑替尼组的无进展生存期较化疗组显著延长(中位值,10.9个月对7.0个月)。两组的客观缓解率分别为74%和45%(P<0.001)。两组的中位总生存期均未达到(克唑替尼组的死亡风险比为0.82)。克唑替尼组的1年生存率为84%,化疗组为79%。克唑替尼组最常见的不良事件包括视觉障碍、腹泻、恶心以及水肿。化疗组最常见的不良事件为恶心、乏力、呕吐和食欲下降。与化疗相比,克唑替尼可以显著减轻肺癌的相关症状并大幅提高生活质量。

交叉用药OS

校正后OS
PROFILE 1029研究[4]:一项随机、开放、双臂III期临床研究,旨在评价在东亚人群(主要是中国人群),克唑替尼一线治疗既往未经过系统性治疗的ALK阳性NSCLC患者的疗效和安全性。PROFILE 1029试验的研究设计与PROFILE 1014相似,研究结果再次证实:与标准含铂类化疗药物相比,克唑替尼一线治疗能够显著延长ALK阳性晚期NSCLC东亚患者的无进展生存期(PFS)。
第二代ALK-TKIs
阿来替尼(Alectinib)
ALEX研究[5](一线):是一项国际性、随机、开放标签的3期试验,在包括无症状CNS转移患者、既往未经治疗的晚期ALK阳性NSCLC患者中,比较了阿来替尼(600 mg,每日2次)与克唑替尼(250 mg,每日2次)。主要终点是无进展生存期。
研究结果:数据截止2017年2月,克唑替尼组和阿来替尼组的中位随访期分别为17.6个月和18.6个月(164起事件)。在布加替尼组和克唑替尼组中,12个月无进展生存率分别为68.4% vs 48.7%,ORR分别为82.9% vs 75.5%;独立审核委员会判定的中位无进展生存期分别为25.7个月和10.4个月(风险比,0.47)。在有可测量病变的患者中,经证实的颅内缓解率分别为81% vs 50%。阿来替尼组3~5级不良事件的发生率较低(阿来替尼组41% vs. 克唑替尼组50%)。





2019年ESMO会议报道,随访37.8个月,研究者评估的PFS分别为34.8个月。

阿来替尼vs布格替尼
阿来替尼、布格替尼均是通过单臂临床试验获批克唑替尼耐药后的后线治疗适应症。阿来替尼治疗克唑替尼耐药患者单臂试验报告的PFS为8.1-10.9个月,布格替尼则高达14.7-16.8个月。为此,武田公司开展了ALTA-3研究。ALTA-3研究[6]是一项3期临床试验,旨在检测布格替尼在克唑替尼治疗后进展的ALK + NSCLC中的疗效是否优于阿来替尼。
研究允许既往接受过≤2种全身方案治疗(不包括除克唑替尼外的其他ALK-TKIs)的晚期NSCLC患者入组。患者按1:1的比例随机接受布格替尼180 mg QD(90 mg剂量下7天导入期)或阿来替尼600 mg BID治疗,并按基线脑转移(BL BM;是/否)和最佳克唑替尼缓解(CR/PR vs其他)分层。主要终点为盲态独立评审委员会(BIRC)评估的PFS;次要终点包括OS、BIRC评估的ORR和安全性。进行了有效性和无效性中期分析,计划在观察到约70%(115起事件)的预期事件(进展或死亡)后进行。
2019年5月至2021年6月,248例患者接受随机分组(布格替尼/阿来替尼,n=125/123);中位年龄:54/53岁;BL BM:64%/61%;既往克唑替尼的最佳缓解CR/PR:67%/69%。在中期分析数据截止时(2022年02月11日),中位随访时间 (布格替尼/阿来替尼) 为15.9/16.9个月,107例 (43%;50/57)发生PFS事件。


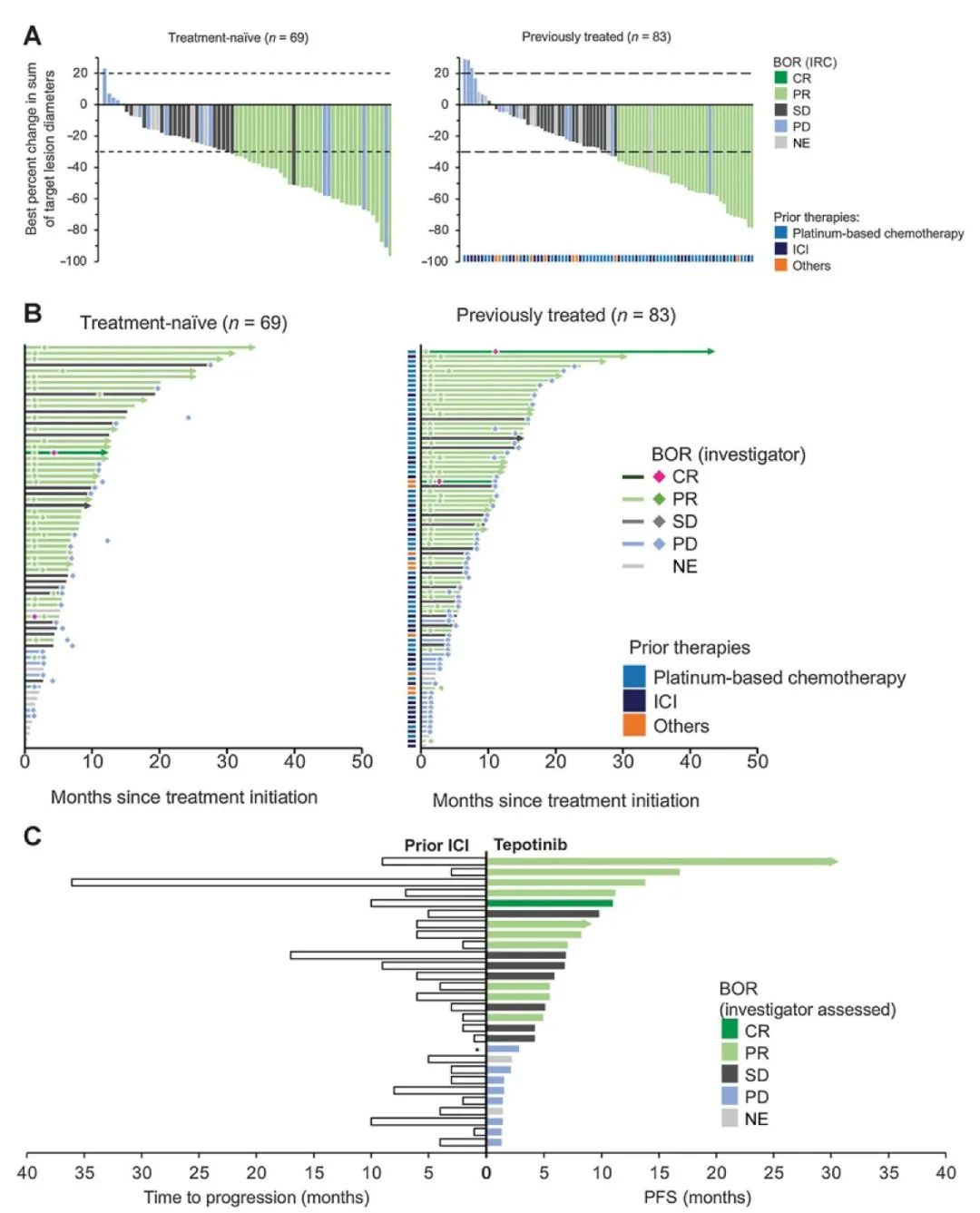
疗效瀑布图

两组安全性
布格替尼(Brigatinib)




赛瑞替尼(Ceritinib)
ASCEND-3研究[9](二线):是一项II期,单臂研究,评估了既往接受≤3种化疗方案且未接受ALK-TKI治疗的患者的疗效及安全性。根据是否合并脑转移,将124例患者分为两组,分别接受色瑞替尼治疗,合并脑转移组、无脑转移组ORR为57.1% vs 74.7%,PFS为10.8vs19.6个月,OS为36.2vs55.3个月。最常见的不良反应包括腹泻(85.5%)、恶心(78.2%)、呕吐(71.8%)、食欲降低(55.6%)及谷丙转氨酶升高(52.4%)。

在ASCEND-4研究中,塞瑞替尼750mg空腹的疗效显著。但使用750mg空腹剂量,有很多患者因为毒性而暂停药物或者进行减量。ASCEND-8研究的设计是要看看减少剂量之后,对塞瑞替尼的疗效和安全性产生了什么样的影响。
ASCEND-8是一个随机对照临床试验、对照组采用了750mg空腹模式,然后再加上两个试验组,一组是600mg,一组是450mg。600mg组和450mg组与750mg最大的不同在于塞瑞替尼是在餐后随餐来使用。所以在这样的剂量下我们主要是看食物对这个药物的影响,是不是有了随餐服用之后能够延缓药物的吸收,让低剂量随餐来达到更好的效果和减少它的毒性。
2020年ESMO年会上,对比塞瑞替尼450mg随餐与750mg空腹疗效和安全性的ASCEND-8研究亚洲人群数据首次向全球公布。截至数据截止(2020年3月6日),74例初治的亚洲患者构成了亚洲亚组(450mg随餐组,n=29;600mg随餐组,n=19;750mg空腹组,n=26)。基线时,450mg随餐组比750mg空腹组有更多的脑转移患者(44.8% vs 26.9%),而除性别、脑转移/骨转移(450mg组脑/骨转移发生率更高)外,各组间亚洲人群基线特征无显著差异,因此,尽管研究为I期临床研究,但各组间具有可比性。数据截止时,亚洲亚组有38名(51.4%)患者仍在进行治疗,停止治疗的最常见的原因是疾病进展(25/74,33.8%)。


亚洲亚组OS

亚组亚组PFS
ASCEND-8研究[12](一线,全球数据):2020年WCLC会议公布了意向治疗(ITT)人群中位随访37.65个月后的更新数据。至2020年3月6日研究结束时,全分析集共包括306名经治和初治的患者,其中疗效分析包括198名初治患者(450mg随餐组,n=73;600mg随餐组,n=51;750mg空腹组,n=74)。三组经研究者评估的客观缓解率(ORR)和疾病控制率(DCR)均较高,其中450mg随餐组的ORR达到75.3%,DCR为94.5%;750mg空腹组的ORR为78.4%,DCR为93.2%。450mg随餐组和750mg空腹组的ORR和DCR相似,但是450mg随餐组的缓解持续时间(DoR)更长,两组分别是未达到和25个月。
恩沙替尼
第三代ALK-TKIs
NEJM丨ALK阳性,三代药劳拉替尼大幅度改善PFS
CROWN研究:一项III期随机CROWN研究(劳拉替尼 vs 克唑替尼)的中期结果显示[15],劳拉替尼在初治ALK阳性晚期NSCLC中可以提高PFS,并且具有颅内活性。2022AACR会议更新报道了36个月的随访数据。自第一次期中分析至2021年9月20日,已继续随访约18.3个月,中位随访时间超过36个月,研究主要终点为盲法独立中心评价(BICR)的PFS。
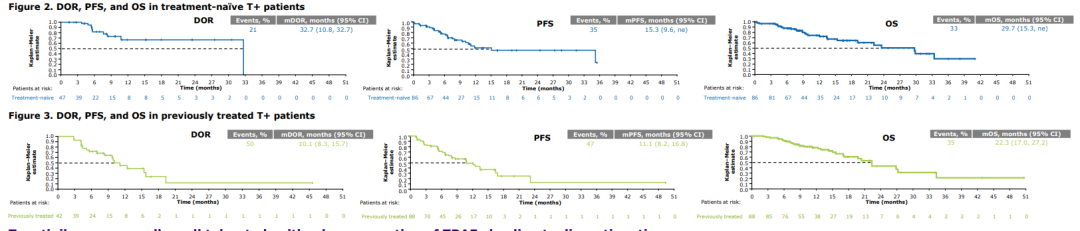
研究结果:劳拉替尼组和克唑替尼组PFS中位随访时间分别为36.7个月和29.3个月,劳拉替尼继续显示出优于克唑替尼的临床疗效,其表现具有突破性意义。基于BICR评估的PFS结果显示:劳拉替尼和克唑替尼中位PFS分别为NR vs 9.3个月(95% CI:0.184-0.388),3年PFS率分别为63.5% vs 18.9%。ALK阳性晚期NSCLC初治患者一线劳拉替尼治疗后,疾病复发或死亡风险较克唑替尼降低73%(HR=0.27)。通过分层分析可以看到,无论是否伴有颅内转移,劳拉替尼都能延长晚期NSCLC患者的PFS。
图1 ITT人群研究结果;图2-3 基线有/无脑转移患者的疗效
颅内控制效力:随访3年时,劳拉替尼组、克唑替尼组ITT人群颅内病变未发生进展的比例分别为92.3% vs 37.7%;脑转移患者中劳拉替尼为72.8%,而克唑替尼组随访18个月后NR。无脑转移患者中,劳拉替尼的表现尤为惊人,仅1例发生颅内进展,远高于克唑替尼组近50%。
安全性:劳拉替尼治疗安全性结果与期中分析结果相似,没有出现新的安全信号事件。劳拉替尼治疗相关AEs主要集中在血脂代谢异常,而克唑替尼治疗相关AEs以消化道症状为主。
第四代ALK-TKIs
ALKOVE-1研究

不良反应
安全性方面,NVL-655耐受性良好,治疗相关不良事件(TRAEs)较轻,最大耐受剂量(MTD)和二期推荐剂量(RP2D)仍未确定。常见的TRAE(≥5%)是转氨酶升高(ALT升高19%,≥3级6%;AST升高18%,≥3级4%)、恶心(10%)、味觉障碍(8%)、便秘(6%)、疲劳/外周水肿(各占5%;外周水肿≥3级1%)。
ALK耐药机制
第一、二代ALK TKI耐药
一二代常见耐药突变



第三代ALK TKI耐药



劳拉替尼治疗前后ALK突变情况[17]
参考文献
[1]Shaw AT, Kim DW, Nakagawa K, et al. Crizotinib versus chemotherapy in advanced ALK-positive lung cancer. N Engl J Med. 2013 Jun 20;368(25):2385-94. doi: 10.1056/NEJMoa1214886.
[2]Solomon BJ, Mok T, Kim DW, et al. First-line crizotinib versus chemotherapy in ALK-positive lung cancer. N Engl J Med. 2014 Dec 4;371(23):2167-77. doi: 10.1056/NEJMoa1408440. Erratum in: N Engl J Med. 2015 Oct 15;373(16):1582.
[3]Solomon BJ, Kim DW, Wu YL, et al. Final Overall Survival Analysis From a Study Comparing First-Line Crizotinib Versus Chemotherapy in ALK-Mutation-Positive Non-Small-Cell Lung Cancer. J Clin Oncol. 2018 Aug 1;36(22):2251-2258. doi: 10.1200/JCO.2017.77.4794.
[4]Wu YL, Lu S, Lu Y, et al. Results of PROFILE 1029, a Phase III Comparison of First-Line Crizotinib versus Chemotherapy in East Asian Patients with ALK-Positive Advanced Non-Small Cell Lung Cancer. J Thorac Oncol. 2018 Oct;13(10):1539-1548. doi: 10.1016/j.jtho.2018.06.012.
[5]Peters S, Camidge DR, Shaw AT, et al. Alectinib versus Crizotinib in Untreated ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med. 2017 Aug 31;377(9):829-838. doi: 10.1056/NEJMoa1704795.
[6]Yang JC, Liu G, Lu S, et al. Brigatinib Versus Alectinib in ALK-Positive NSCLC After Disease Progression on Crizotinib: Results of Phase 3 ALTA-3 Trial. J Thorac Oncol. 2023 Aug 12:S1556-0864(23)00730-X. doi: 10.1016/j.jtho.2023.08.010.
[7]Camidge DR, Kim HR, Ahn MJ, et al. Brigatinib versus Crizotinib in ALK-Positive Non-Small-Cell Lung Cancer. N Engl J Med. 2018 Nov 22;379(21):2027-2039. doi: 10.1056/NEJMoa1810171.
[8]Camidge DR, Kim HR, Ahn MJ, et al. Brigatinib Versus Crizotinib in Advanced ALK Inhibitor-Naive ALK-Positive Non-Small Cell Lung Cancer: Second Interim Analysis of the Phase III ALTA-1L Trial. J Clin Oncol. 2020 Nov 1;38(31):3592-3603. doi: 10.1200/JCO.20.00505.
[9]Nishio M, Felip E, Orlov S, et al. Final Overall Survival and Other Efficacy and Safety Results From ASCEND-3: Phase II Study of Ceritinib in ALKi-Naive Patients With ALK-Rearranged NSCLC. J Thorac Oncol. 2020 Apr;15(4):609-617. doi: 10.1016/j.jtho.2019.11.006.
[10]Soria JC, Tan DSW, Chiari R, et al. First-line ceritinib versus platinum-based chemotherapy in advanced ALK-rearranged non-small-cell lung cancer (ASCEND-4): a randomised, open-label, phase 3 study. Lancet. 2017 Mar 4;389(10072):917-929. doi: 10.1016/S0140-6736(17)30123-X.
[11]Byoung Chul Cho, Dong-Wan Kim, Scott Laurie, et al. Efficacy and Safety of Ceritinib 450-mg Fed vs 750-mg Fasted in Patients With ALK+ NSCLC: Final Report of the ASCEND-8 Study. 2020 WCLC Abs P84.05.
[12]Byoung Chul Cho, Dong-Wan Kim, Ullas Batra, et al. Efficacy and safety of ceritinib 450 mg-fed vs 750 mg-fasted in Asian patients (pts) with ALK+ non-small cell lung cancer (NSCLC) in the ASCEND-8 trial. 2020 ESMO Abs 1348P.
[13]Yang Y, Zhou J, Zhou J, et al. Efficacy, safety, and biomarker analysis of ensartinib in crizotinib-resistant, ALK-positive non-small-cell lung cancer: a multicentre, phase 2 trial. Lancet Respir Med. 2020 Jan;8(1):45-53. doi: 10.1016/S2213-2600(19)30252-8.
[14]Selvaggi G, Wakelee HA, Mok T, et al. Phase III randomized study of ensartinib vs crizotinib in anaplastic lymphoma kinase (ALK) positive NSCLC patients: EXALT3. Presented at the International Association for the Study of Lung Cancer World Conference on Lung Cancer, Singapore, August 8, 2020. abstract.
[15]Shaw AT, Bauer TM, de Marinis F, et al. First-Line Lorlatinib or Crizotinib in Advanced ALK-Positive Lung Cancer. N Engl J Med. 2020 Nov 19;383(21):2018-2029. doi: 10.1056/NEJMoa2027187.
[16]Shaw AT, Solomon BJ, Besse B, et al. ALK Resistance Mutations and Efficacy of Lorlatinib in Advanced Anaplastic Lymphoma Kinase-Positive Non-Small-Cell Lung Cancer. J Clin Oncol. 2019 Jun 1;37(16):1370-1379. doi: 10.1200/JCO.18.02236.
[17]Yoda S, Lin JJ, Lawrence MS, et al. Sequential ALK Inhibitors Can Select for Lorlatinib-Resistant Compound ALK Mutations in ALK-Positive Lung Cancer. Cancer Discov. 2018 Jun;8(6):714-729. doi: 10.1158/2159-8290.CD-17-1256.